Importancia
La neuropatía periférica, definida como daño a los nervios periféricos, afecta aproximadamente al 1% de los adultos en todo el mundo.
La prevalencia aumenta con la edad y se ha estimado que afecta entre el 6% y el 10% de la población mayor de 60 años.
Existen más de 200 causas de neuropatía periférica, con síntomas que varían en gravedad, desde un leve entumecimiento de los dedos del pie hasta síntomas debilitantes que pueden requerir silla de ruedas.
La diabetes es la causa más común y afecta a aproximadamente 206 millones de personas en todo el mundo. (Ver publicación de Septiembre)
Observaciones
La neuropatía periférica típicamente depende de la longitud, lo que significa que los síntomas aparecen en los axones nerviosos más largos (dedos de los pies) y progresan proximalmente con el tiempo.
La neuropatía periférica longitud dependiente (NPLD), también conocida como polineuropatía simétrica distal , es el tipo más común que atendemos los médicos de familia y presenta características predominantemente sensitivas que motoras.
Suele comenzar en los dedos de los pies y puede progresar lentamente proximalmente hacia las rodillas y las manos.
Típicamente es simétrica y afecta a los axones sensoriales más que a los motores.
La neuropatía diabética, que a menudo se asocia tanto con síntomas sensoriales, como dolor, hormigueo o entumecimiento; debilidad leve; y síntomas autonómicos, como hipotensión ortostática, representa más del 50% de la neuropatía periférica en las poblaciones occidentales.
Otras causas de neuropatías incluyen causas hereditarias, como la enfermedad de Charcot-Marie-Tooth, neuropatía tóxica por medicamentos (quimioterapias [p. ej., cisplatino, paclitaxel, vincristina], amiodarona o inhibidores de la transcriptasa inversa de nucleótidos del VIH [p. ej., estavudina, zalcitabina]); alcohol; deficiencias vitamínicas como la vitamina B 12 ; y gammapatías monoclonales.
Hasta el 27% de los adultos con neuropatía no presentan una etiología identificable tras las pruebas diagnósticas.
La neuropatía periférica resulta del daño a las neuronas sensitivas, motoras y autónomas ( Fig. 1 ).
La hiperglucemia crónica daña los nervios periféricos a través de diversos mecanismos bioquímicos, vasculares e inflamatorios interrelacionados.
Las células de Schwann, que mielinizan axones grandes o envuelven fibras amielínicas pequeñas, mantienen la salud axonal mediante factores de crecimiento (p. ej., factor de crecimiento nervioso, factor neurotrófico derivado del cerebro, factor de crecimiento endotelial vascular) y regulando el metabolismo axonal del hierro y el lactato.
El daño a las células de Schwann ralentiza la conducción y puede contribuir a la degeneración axonal.
Las neuropatías se desarrollan cuando las neuronas mueren, los axones se degeneran, la excitabilidad neuronal se altera o falla el soporte de las células de Schwann.
Si se preserva la supervivencia neuronal, la regeneración axonal puede ocurrir a una velocidad de 1 a 3 mm por día después de que se corrija la causa de la lesión.
La NPLD generalmente se manifiesta principalmente como signos y síntomas sensoriales, como entumecimiento y parestesia, indicativos de daño a los axones sensoriales de fibras grandes involucrados en la propiocepción y la sensación de vibración y/o los axones sensoriales de fibras pequeñas responsables de las sensaciones de temperatura y dolor.
El predominio sensorial de la NPLD no se comprende completamente, pero puede deberse en parte a la presencia de capilares fenestrados en los ganglios de la raíz dorsal, que reducen la barrera hematoneuronal y aumentan la susceptibilidad a factores sistémicos como la hiperglucemia o la exposición a medicamentos neurotóxicos.
Los axones que inervan los dedos de los pies pueden medir hasta 92 cm de largo y requieren un alto soporte metabólico para el transporte axonal, lo que explica por qué la PNLD afecta primero los dedos de los pies y luego la parte inferior de las piernas y las manos.
Fig. 1
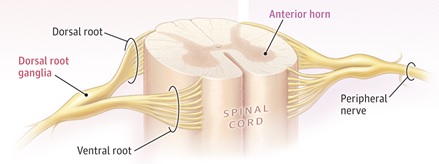
Los axones de las neuronas motoras son principalmente de gran diámetro y mielinizados. Los axones de las neuronas sensoriales varían desde grandes mielinizados, pequeños mielinizados o pequeños amielínicos.

¿Hay lesión de los axones de las neuronas autónomas?
Sí! los mismos tienen axones pequeños amielínicos.
Puede haber síntomas como falta de sudoración en los pies, y aquellos con diabetes o amiloidosis pueden experimentar mareos posturales, ojos secos/boca seca, náuseas y vómitos posprandiales, diarrea, estreñimiento y disfunción eréctil.
La neuropatía periférica puede deberse a un daño primario en el axón, que se manifiesta con mayor frecuencia como degeneración walleriana, o a un daño primario en la mielina, que se manifiesta con mayor frecuencia como desmielinización. (Fig. 2)
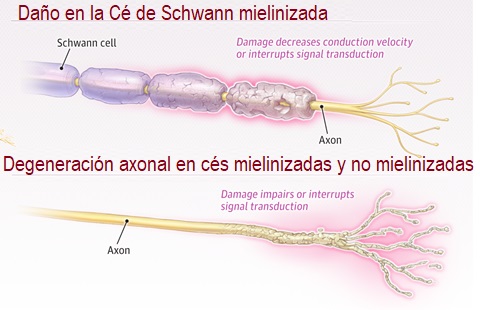
Por lo general, la afectación inicial es la función sensorial de un nervio periférico y progresa lentamente durante semanas o meses de manera simétrica.
Los síntomas suelen ser pérdida sensorial (entumecimiento) y parestesias (hormigueo, picor) que comienzan en los dedos de los pies y los pies. Puede presentarse dolor neuropático (p. ej., ardor, punzadas, descargas eléctricas, hiperalgesia, alodinia).
A medida que progresa la neuropatía, los síntomas se extienden proximalmente hasta la parte inferior de las piernas.
Los pacientes con síntomas hasta las rodillas a menudo informan síntomas en las yemas de los dedos porque la longitud de los nervios hasta las yemas de los dedos es similar a la distancia de los nervios hasta las rodillas.
Cuando está presente, la debilidad motora comienza en los dedos de los pies con debilidad de flexión y extensión y suele ser leve.
Los médicos debemos evaluar a los pacientes para detectar causas comunes de este cuadro como diabetes, alcoholismo, afecciones asociadas con la deficiencia de vitamina B12 ( enfermedad inflamatoria intestinal, enfermedad celíaca, cirugía bariátrica y falta de consumo de carne, aves y huevos).
Los medicamentos que pueden afectar la función nerviosa periférica incluyen quimioterapias como paclitaxel, vincristina y cisplatino, piridoxina (vitamina B6 ) , amiodarona y tratamientos relacionados con el VIH, como inhibidores de la transcriptasa inversa de nucleótidos, como la estavudina y la zalcitabina
Se debe determinar si los pacientes presentan deformidades en los pies, como pie cavo (arco pronunciado) o dedos en martillo (dedos encorvados), y si utilizan ayudas para caminar.
También hay que interrogar sobre antecedentes familiares, incluyendo preguntas sobre antecedentes familiares de síntomas de neuropatía.
Aproximadamente entre un tercio y la mitad de todas las neuropatías idiopáticas son probablemente hereditarias, siendo la más común la enfermedad de Charcot-Marie-Tooth.
Se debe evaluar
a. la sensibilidad comenzando en el dorso del dedo gordo del pie y el índice y moviéndose proximalmente hacia arriba por la pierna y el brazo hasta que se establezca un nivel de sensibilidad normal.
b. la función de las fibras grandes (vibración, propiocepción y tacto ligero) y de las fibras pequeñas (pinchazo y temperatura).
c. La presencia del signo de Romberg (inestabilidad con los pies juntos, los brazos extendidos y los ojos cerrados) indica un deterioro de la propiocepción.
d. El examen motor puede mostrar atrofia intrínseca del pie y debilidad en la flexión/extensión de los dedos, y puede afectar los tobillos y las manos.
e. Los reflejos tendinosos profundos del tobillo suelen estar reducidos o ausentes.
f. Aunque la marcha es normal cuando hay leve predominio sensorial, aquellos con neuropatía más grave pueden tener una marcha inestable y de base amplia debido a la pérdida sensorial propioceptiva de las fibras grandes (ataxia sensorial).
Los pacientes con enfermedad de Charcot-Marie-Tooth generalmente presentan debilidad distal en el pie y el tobillo, ausencia de síntomas sensoriales neuropáticos positivos (hormigueo, ardor, eléctricos) y presencia de pie cavo y dedos en martillo.
Las características atípicas de la NPLD incluyen debilidad motora grave; síntomas autonómicos prominentes como intolerancia ortostática, náuseas posprandiales, vómitos y diarrea; aparición y progresión de los síntomas a lo largo de días o semanas (en lugar de un inicio más lento); patrones de pérdida sensorial o debilidad no dependientes de la longitud; asimetría de la neuropatía; y presencia de pérdida de peso, fiebre, sarpullido y afectación de otros sistemas orgánicos.
Estas características pueden estar asociadas a un proceso inmunitario, inflamatorio, infeccioso o neoplásico, lo que debe llevar a una interconsulta con un neurólogo y, posiblemente, a otros especialistas (reumatología, enfermedades infecciosas, oncología) para facilitar la evaluación.
No reconocer las presentaciones atípicas puede provocar un retraso en el tratamiento y peores resultados.
Recordá!
La falta de sensibilidad puede provocar lesiones no diagnosticadas (quemaduras, cortes) que pueden ulcerarse e infectarse.
Los pacientes con diabetes también pueden presentar enfermedad microvascular concurrente que dificulta la cicatrización de las heridas.
Para mitigar las complicaciones derivadas de la pérdida de sensibilidad, los propios pacientes deben inspeccionarse los pies a diario, usar calzado adecuado para evitar ampollas y comprobar la temperatura del agua con las manos antes de sumergir los pies en agua caliente.
Considerar la consulta con un podólogo en pacientes con alto riesgo de úlceras en los pies (p. ej., pacientes con diabetes).
Recordá! El diagnóstico se basa en los signos y síntomas clínicos.
Las pruebas de laboratorio pueden identificar etiologías específicas asociadas con NPLD, como diabetes, deficiencia de vitamina B12 o gammapatías monoclonales
Las pruebas recomendadas incluyen glucosa en sangre, vitamina B12 sérica con metabolitos (ácido metilmalónico con o sin homocisteína) y electroforesis de proteínas séricas con inmunofijación.
Si no se identifica una etiología y la prueba de rutina de glucosa en sangre en ayunas es normal, se pueden considerar otras pruebas para prediabetes o diabetes, como la hemoglobina A1C o una prueba de tolerancia a la glucosa, especialmente si la neuropatía periférica está acompañada de dolor.
Los estudios electrodiagnósticos, que consisten en estudios de conducción nerviosa para evaluar los nervios de fibras grandes y electromiografía (EMG), pueden ayudar a diagnosticar la neuropatía periférica.
Los hallazgos que sugieren NPLD incluyen
(1) afectación precoz y más grave de los nervios sensitivos que de las fibras motoras;
(2) afectación precoz y más grave de la conducción en las extremidades inferiores que en las superiores; y
(3) anomalías simétricas de la conducción en nervios de longitud similar.
También puede ayudar a identificar la fisiopatología subyacente (es decir, axonal o desmielinizante).
Las características axonales incluyen respuesta de amplitudes motoras y sensitivas reducidas en la conducción y potenciales de unidad motora neurogénica en el EMG.
Los hallazgos de la conducción que sugieren desmielinización incluyen velocidades de conducción lentas, latencias distales prolongadas, bloqueo de la conducción y dispersión temporal.
La mayoría de las neuropatías dependientes de la longitud son axónicas, incluyendo la diabetes, la deficiencia de vitamina B12 , la neuropatía periférica inducida por quimioterapia y el subtipo axonal de Charcot-Marie-Tooth tipo 2.
Aunque se recomiendan pruebas electrodiagnósticas para pacientes con neuropatías periféricas que presentan características atípicas, las pruebas electrodiagnósticas para diagnosticar NPLD simétrica son controvertidas.
La Asociación Americana de la Diabetes declaró que el EMG de rutina no es necesario en pacientes con diabetes que presentan una neuropatía simétrica.
Sin embargo, el EMG puede cambiar el diagnóstico o el tratamiento en el 24% al 43% de los pacientes sometidos a evaluación por neuropatía periférica.
Incluye pacientes con signos y síntomas típicos de neuropatía.
Las pruebas electrodiagnósticas pueden identificar otras afecciones que pueden presentarse de forma similar a la neuropatía periférica, como las neuropatías compresivas y las radiculopatías lumbosacras, que requieren una evaluación y un tratamiento diferentes.
Ligandos de la subunidad α2-δ del canal de calcio, como la gabapentina y la pregabalina
Inhibidores de la recaptación de serotonina y noradrenalina, como la duloxetina y la venlafaxina;
Antidepresivos tricíclicos, como la amitriptilina y la nortriptilina.
El dolor a menudo persiste a pesar del tratamiento médico.
Se observó al menos una reducción del 50% en el dolor en el 38% de aquellos con neuropatía periférica diabética dolorosa que recibieron 1200 mg de gabapentina al día.
En cuanto a los síntomas motores, las personas con debilidad en las extremidades inferiores debido a neuropatía periférica pueden tener una marcha deteriorada debido a una combinación de debilidad y pérdida sensorial propioceptiva, lo que conduce a un mayor riesgo de caídas.
La fisioterapia centrada en la seguridad de la marcha puede ser útil para pacientes con debilidad leve.
La terapia ocupacional está indicada para pacientes con debilidad en las extremidades superiores, especialmente si los movimientos finos de las manos (p. ej., abotonarse, escribir, autocuidado) están alterados.
Si hay deformidades y contracturas en los pies pueden beneficiarse con cirugía ortopédica.
El pronóstico de la neuropatía periférica varía según su causa.
Incluso en neuropatías periféricas tratables, como vasculitis y amiloidosis, el daño a los nervios periféricos no puede revertirse por completo y los síntomas casi siempre persisten.
De igual manera, las neuropatías causadas por toxinas o quimioterapia pueden mejorar con la interrupción del agente causal, pero los síntomas a menudo persisten.
Si bien alcanzar la normoglucemia puede prevenir la NPLD en personas con DBT tipo 1, el control glucémico tiene efectos moderados en la mejora de los síntomas de la neuropatía periférica en aquellos con neuropatía periférica establecida debido a la diabetes tipo 2.
Las neuropatías hereditarias de inicio tardío, incluyendo los tipos axónicos de Charcot-Marie-Tooth, generalmente no causan discapacidad grave, pero pueden afectar negativamente la marcha en pacientes con otros problemas relacionados con la edad, como osteoartritis, reducción de la visión/audición o enfermedades del sistema nervioso central como el accidente cerebrovascular o la enfermedad de Parkinson.
Referencia
Publicado en JAMA el 17-11-2025
doi: 10.1001/jama.2025.19400
![]()

